Introducción
Actualmente
vivimos la pandemia causada por el virus
SARS- CoV- 2; sin embargo, estamos frente a una amenaza cada vez mayor para la
salud mundial, la resistencia a los antibióticos. De acuerdo con Barco (2021)
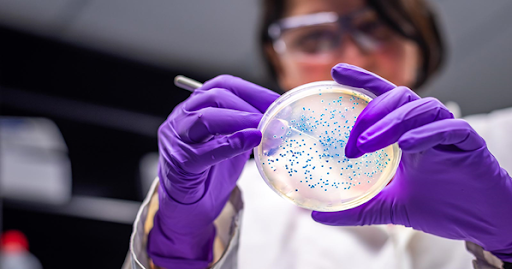
solo en el año 2015 las bacterias
resistentes a los antibióticos provocaron 670.000 infecciones y 33.110 muertes; la OMS pronostica que serán 10 millones las personas fallecidas en
el año 2050 por esta causa. En esta línea, Guevara et al. (2022) señala que
se estima que para las próximas décadas,
el número de muertes a causa de patógenos multirresistentes será mayor que las
muertes causadas por cáncer.
Lo
anterior supone la búsqueda de tratamientos alternativos para controlar
enfermedades causadas por estos microorganismos. Si bien la resistencia a los
antibióticos corresponde a un fenómeno natural, el que para Guevara et al.
(2022) ocurre como una respuesta evolutiva a la fuerte presión selectiva dada
principalmente por la exposición e interacción
de los microrganismos a agentes
químicos (desinfectantes y metales pesados entre otros) lo cual acelera el traspaso
de genes de resistencia en las poblaciones bacterianas aledañas, produciendo
un aumento en el número de patógenos multirresistentes con ventajas
evolutivas y adaptativas.
Por
otro lado, el autor señala la existencia
de una relación directa entre el consumo de antibióticos y las variaciones de
resistencia que producen estos medicamentos en los microorganismos. Es así que para comprender la evolución y el
impacto de la resistencia microbiana surge
el concepto de “resistoma”, el
cual que incluye a todos los genes de resistencia a los antibióticos y a sus
precursores (en bacterias patógenas como no patógenas), lo que permite entender
e investigar los orígenes y evolución de
la resistencia.
Bacteriófagos ¿Qué son?
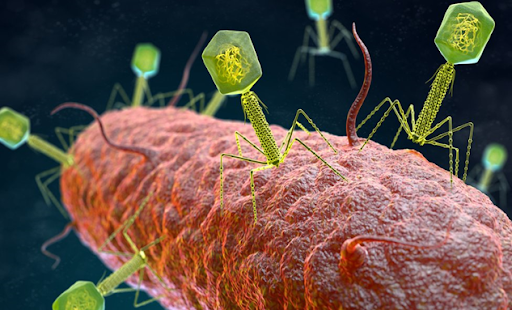
Los
bacteriófagos son virus que infectan a bacterias, como afirma Sejas (2021)
se encuentran entre los organismos más abundantes y ubicuos de nuestro
planeta, son catalogados como controladores naturales de las bacterias. De
acuerdo con Guevara et al. (2022) cada bacteria tiene sus fagos
específicos, los que podrían utilizarse
como agentes antibacterianos. Pero, no piensen que los bacteriófagos al ser específicos nos puedan atacar, el que sean específicos significa que solo pueden atacar a una especie puntual, que son las bacterias, no a los seres humanos; como super héroes no atacan a los buenos, sino que solo a los villanos.
Cabe señalar también, que los bacteriófagos debido a su especificidad, son usados en otros ámbitos, por ejemplo, el agropecuario y alimenticio. Para saber más revisa: https://aes.ucf.edu.cu/index.php/aes/article/view/18
https://scielo.conicyt.cl/scielo.php?pid=S0716-10182015000700010&script=sci_arttext&tlng=n
Barco (2021) indica que el 96% de los fagos conocidos pertenecen a tres familias: Podoviridae, Myoviridae y Siphoviridae. Los bacteriófagos fueron descubiertos en el año 1915, por el microbiólogo inglés Frederick Twort, este identificó un agente bacteriolítico que infectaba y mataba bacterias, pero sin lograr definirlo; no fue hasta 1917 que el microbiólogo canadiense Félix d'Herelle informó el descubrimiento de "un invisible antagonista microbiano del bacilo de la disentería" y confirmó que se trataba de un virus al que llamó "bacteriófago".
Para saber más: https://elpais.com/elpais/2019/05/23/ciencia/1558629279_769979.html
Morfología
Citando
a Aties et al. (2017) los fagos se constituyen fundamentalmente de material
genético y proteínas. Su genoma puede ser de ácido desoxirribonucleico (ADN) o
ácido ribonucleico (ARN), el cual puede ser unicatenario o bicatenario; este
material genético se encuentra protegido por una cubierta de proteínas
denominada cápside.
La
estructura de los fagos es determinada por sus proteínas de envoltura, cuya
función es la de proteger al material genético; estas proteínas además cumplen el rol de proporcionar al fago:
cuello, cola, fibras caudales, láminas
básales y/o espículas.
Morfológicamente los bacteriófagos son virus con cola y receptores para el reconocimiento bacteriano. En las familias Myoviridae y Siphoviridae las colas son largas, contráctiles para la primera y no contráctiles para la segunda familia; y en la familia Podoviridae las colas son cortas y no contráctiles (Barco, 2021). Los bacteriófagos miden entre 50 y 200 nm (Richter et al., 2018) citado por Fuentes et al. (2021) y sólo pueden ser visibles con un microscopio electrónico.
Créditos de la imagen: https://www.google.com/url?sa=i&url=https%3A%2F%2Fwww.bbc.com%2Fmundo%2Fvert-fut-55714386&psig=AOvVaw2C9N33u_xzDFzYGl8Fcx9g&ust=1645737606634000&source=images&cd=vfe&ved=2ahUKEwje8uG84Jb2AhW0N7kGHY7DANEQr4kDegUIARD6AQ
Ciclo de vida de un fago
Barco
(2021) indica que los bacteriófagos presentan dos ciclos de vida, el ciclo lítico
y el ciclo lisogénico; aunque hay que
hacer la salvedad, según Aties et al. (2017) que no todos los bacteriófagos
pueden usarse en terapia, únicamente los pertenecientes al ciclo lítico, dado
que los fagos con ciclo lisogénico, al integrar su genoma en el de la bacteria,
no la matan y pueden incluso transferir genes que incrementen la virulencia de
la bacteria.
El
ciclo lítico se divide en cinco fases:
primero se produce la adsorción de fagos a la célula huésped mediante la unión
a receptores específicos de la superficie bacteriana (1). Luego, el fago
inyecta el material genético en la bacteria mediante la contracción de la
cola y la formación de un agujero en la
pared celular (2). Estos genes se
expresan y la bacteria los replica originando varias copias del genoma vírico (3). Las proteínas estructurales de
los nuevos viriones se ensamblan formando partículas fágicas (4), finalmente se degrada la pared bacteriana por acción de
proteínas del fago (5), se produce la lisis y liberación de la progenie viral.
En este último proceso, la mayoría de
fagos utiliza dos grupos de proteínas: holinas y endolisinas, que forman
sistemas holin-lisina, causantes de la lisis.
Créditos: https://www.google.com/url?sa=i&url=https%3A%2F%2Fwww.researchgate.net%2Ffigure%2FFigura-1-Esquema-general-del-ciclo-litico-de-un-fago-1-Adsorcion-a-la-superficie_fig2_294275865&psig=AOvVaw1mO3s_OaGscKQTjU6AStAU&ust=1645738013056000&source=images&cd=vfe&ved=2ahUKEwiz98f-4Zb2AhUpBLkGHT-8CyUQr4kDegUIARDsAQ
¿Cómo
actúan?
Además de sacar
provecho terapéutico al ciclo lítico del bacteriófago, existen otras técnicas. De acuerdo
con Fuentes et al. (2021) las endolisinas, enzimas que degradan la pared
celular bacteriana, actúan como enzibióticos
(enzimas con actividad antibiótica); estas enzimas también son útiles en el control de las
biopelículas (acumulaciones de bacterias que secretan moléculas que las
protegen y que dificultan la efectividad de los antibióticos) y además se usan
en la desinfección de equipo hospitalario y en la industria alimentaria.
También se pueden
usar solamente las proteínas de la cápside del bacteriófago para construir partículas tipo virus (vlps, por sus siglas
del inglés Viral Like Particles), las cuales sirven para el diseño de vacunas
contra infecciones virales, las que al carecer de material genético son
seguras para la inducción de anticuerpos neutralizantes, por ejemplo, contra la
influenza.
Por último, las
endolisinas se utilizan para generar “fantasmas bacterianos” (Bacterial Ghosts
o bgs, en inglés), estos son células bacterianas que perdieron su contenido
celular, quedando solamente la envoltura.
Créditos: https://www.google.com/url?sa=i&url=https%3A%2F%2Fwww.ocu.org%2Falimentacion%2Fseguridad-alimentaria%2Finforme%2Fbacteriofagos&psig=AOvVaw3oMxbJUO1tB64HR8Bf7kxa&ust=1645738136984000&source=images&cd=vfe&ved=2ahUKEwjp-NO54pb2AhUECrkGHZCUCcIQr4kDegQIARBj
Pros y
contras de la terapia con fagos.
Como lo hace notar Fuentes
et al. (2021) la terapia de bacteriófagos presenta numerosas ventajas en
comparación con la terapia con antibióticos convencionales, algunas de ellas son:
1) Son abundantes en
la naturaleza y de bajo costo, un solo bacteriófago puede aniquilar a un gran número de bacterias.
2) Los
bacteriófagos líticos destruyen por completo a las bacterias.
3) Son muy
específicos, infectan únicamente a su bacteria hospedera, dejando intactas a
otras bacterias benéficas y no infectan a los humanos, animales o plantas.
4) Una sola dosis
es suficiente para el control de la infección bacteriana, ya que mientras hayan
bacterias, los bacteriófagos continuarán
replicándose y una vez eliminadas, también dejarán de multiplicarse.
5) Pueden mutar
para evadir las defensas de las bacterias. Se pueden utilizar mezclas de bacteriófagos
para evitar el desarrollo de resistencia bacteriana.
6) No causan alergias como lo hacen algunos antibióticos
Aties et al.
(2017), plantea como dificultad
para el uso de bacteriófagos que pueden
producir altos niveles de endotoxinas en infecciones causadas por bacterias gram negativas.
Conclusión
Actualmente,
la evidencia en relación al potencial terapéutico que presentan los bacteriófagos ha demostrado
efectos positivos en un alto porcentaje de los casos reportados; sin embargo, se debe
seguir investigando en un universo mayor a fin de terminar de estudiar aspectos que permitan estandarizar el manejo terapéutico
y convertir esta terapia en una realidad frente a las bacterias multirresistentes.
Aties L., Duret, Y., Tabares, M., Fernández, S. (2017). Los enzibióticos como alternativa terapéutica contra las enfermedades bacterianas. MEDISAN. 21(10) ,3077
Barco, P. (2021).Terapia fágica como alternativa a la resistencia a antibióticos. NPunto, 5(35), 142-146
Fuentes, M., Gil, A., Martínez, C., Baizabal, V., Valdez, J. (2021). El enemigo de mi enemigo es… Un virus que ataca a las bacterias: los bacteriófagos. Revista Digital Universitaria. 22(4) ,1-13 http://doi.org/10.22201/cuaieed.16076079e.2021.22.4.1
Guevara, F., Muñoz Molina, L., Navarrette, J., Salazar, L., Pinilla, G. (2020). Innovaciones
en la terapia antimicrobiana. NOVA. 18 (34), 09-25







No hay comentarios:
Publicar un comentario
Gracias por comentar.
Recibirás pronta respuesta y si lo deseas, información extra sobre el tema.